Těžká akutní forma imunitní trombocytopenické purpury u nezletilé těhotné
Acute immune trobocytopenic purpura in pregnant adolescent
Objective: The article reviews the causes of thrombocytopenia in pregnancy and the basic examination scheme. Further, it deals in more details with diagnosis of immune thromocytopenic purpura (ITP) and presents a case report of a rare case of acute severe ITP in pregnant adolescent.
Design: Review article and case report.
Settings: Department Obstet/Gynecol Uni J. A. Purkyně and Masaryk´s Hospital, Ústí nad Labem; Children and adolescent dep. Hospital Most; Institute of Hematology and Blood Transfusion Prague; Department of Children Med. Uni J. A. Purkyně and Masaryk´s Hospital, Ústí nad Labem; Department of Clinic Hematology Masaryk´s Hospital, Ústí nad Labem; Department of Neonatology Uni J. A. Purkyně and Masaryk´s Hospital, Ústí nad Labem.
Methods: Based on a review of the published papers, general rules for diagnosis, treatment, fetal risks, pregnancy management and labor in women with immune thrombocytopenic purpura (ITP) are given. Further we present the case of a 16-year-old pregnant girl with an acute severe form of ITP not responding to corticosteroid treatment who underwent twice critical decline of platelets up to 1×109 and repeatedly it was necessary to access the application of IVIG and Azathioprim (Imuran) was also used in her treatment. Pregnancy was unplanned terminated for dg. placental abortion in gestational age 32+4.The girl of 1740 g/42 cm was born with Apgar score 10–10–10 with no signs of thrombocytopenia. Surgery and postoperative course in the mother without complications. The newborn was discharged from the hospital into home care at a gestational age of 36+1 along with his mother.
Results: We present a case of acute severe form of ITP in pregnancy with a successful though somewhat dramatic end.
Conclusions: These rare cases are demanding in terms of logistical, personnel and material provision. The aim of the treatment is to achieve a satisfactory maturity of the fetus, the treatment is financially demanding and is not without risks. Therefore, these cases should only be dealt with at Perinatology Centers in close cooperation with hematologists and neonatologists.
Keywords:
pregnancy – immune trobocytopenic purpura
Authors:
T. Binder 1; J. Biolek 2; A. Srbová 3; D. Procházková 4; A. Vašková 5; F. Fadi 1; M. Pánek 6
Authors‘ workplace:
Gynekologicko-porodnická klinika UJEP a Masarykovy nemocnice, Ústí nad Labem, přednosta doc. MUDr. T. Binder, CSc.
1; Dětské a dorostové oddělení nemocnice Most, primářka MUDr. M. Váchová
2; Ústav hematologie a krevní transfuze, Praha, ředitel prof. MUDr. P. Cetkovský, Ph. D., MBA
3; Dětská klinika UJEP a Masarykovy nemocnice, Ústí nad Labem, přednosta MUDr. J. Škvor, CSc.
4; Oddělení klinické hematologie Masarykovy nemocnice, Ústí nad Labem, primářka MUDr. J. Ullrychová
5; Neonatologická klinika UJEP a Masarykova nemocnice, Ústí nad Labem, přednosta MUDr. P. Hitka, Ph. D.
6
Published in:
Ceska Gynekol 2019; 84(6): 443-449
Category:
Overview
Cíl studie: Článek uvádí v přehledu příčiny trombocytopenie v těhotenství a základní vyšetřovací schéma. Dále se podrobněji zabývá diagnózou imunitní tromocytopenické purpury (ITP) a prezentuje kazuistiku raritního případu akutní těžké formy ITP u těhotné adolescentky.
Typ studie: Přehledový článek a kazuistika.
Název a sídlo pracoviště: Gynekologicko-porodnická klinika UJEP a Masarykovy nemocnice, Ústí nad Labem; Dětské a dorostové oddělení nemocnice Most; Ústav hematologie a krevní transfuze, Praha; Dětská klinika UJEP a Masarykovy nemocnice, Ústí nad Labem; Oddělení klinické hematologie Masarykovy nemocnice, Ústí nad Labem; Neonatologická klinika UJEP a Masarykova nemocnice, Ústí nad Labem.
Metodika: Na základě review publikovaných prací jsou uvedena obecná pravidla diagnostiky, léčby, rizik pro plod, managementu těhotenství a vedení porodu u žen s imunitní trombocytopenickou purpurou. Dále je prezentován případ těhotenství 16leté dívky s akutní těžkou formou ITP nereagující na léčbu kortikoidy, která prodělala dvakrát kritický pokles trombocytů až 1×109 a opakovaně bylo nutné přistoupit k léčbě IVIG a v léčbě byl použit i azathioprim (Imuran). Těhotenství bylo neplánovaně ukončeno pro dg. abrupce placenty v gestačním stáří 32+4. Porozeno bylo děvče 1740 g, Apgar skóre 10–10–10, bez známek trombocytopenie. Operační výkon i další pooperační průběh u matky bez komplikací. Dítě bylo spolu s matkou propuštěno do domácí péče v gestačním stáří 36+1.
Výsledky: Prezentujeme případ akutní těžké formy ITP v graviditě s úspěšným, i když poněkud dramatickým koncem.
Závěry:Tyto raritní případy jsou náročné na logistické, personální a materiální zajištění. Cílem léčby je dosažení uspokojivé maturity plodu, léčba je finančně náročná a není bez rizik. Proto by tyto případy měly být řešeny výhradně v perinatologických centrech v úzké spolupráci s hematology a neonatology.
Klíčová slova:
imunitní trombocytopenická purpura – těhotenství
ÚVOD
Trombocytopenie patří mezi nejčastější hematologické poruchy komplikující přibližně 10 % těhotenství. Její příčiny jsou různé, některé jsou výhradně spojeny s těhotenstvím, některé se objevují v těhotenství ve zvýšené frekvenci a některé nemají s těhotenstvím žádnou příčinnou souvislost (tab. 1). Některé trombocytopenie nejsou spojovány s nežádoucími perinatálními výsledky, zatímco jiné signifikantně ohrožují matku, plod a novorozence. Doba vzniku a manifestace klinických příznaků se u jednotlivých příčin trombocytopenie často překrývají, a činí tak stanovení správné diagnózy obtížnější (tab. 2).
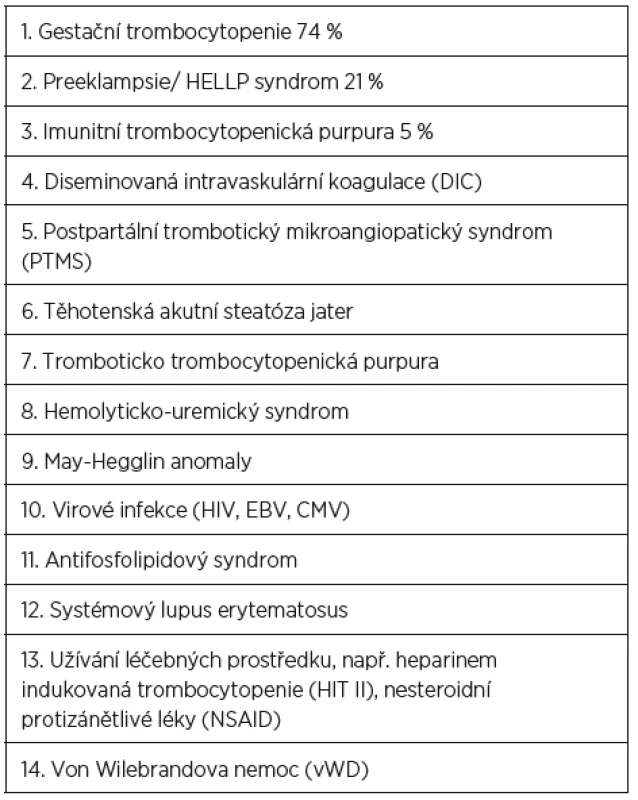
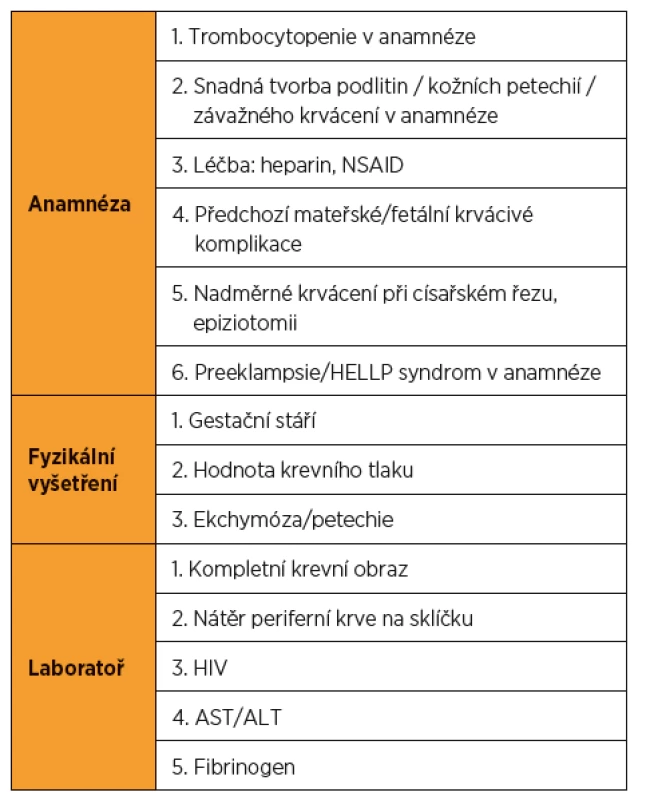
Léčba trombocytopenie je primárně závislá na vyvolávající příčině. Včasné a přesné určení diagnózy je tedy zásadní. Vždy konzultujeme hematologa. V 75 procentech případů se jedná o benigní těhotenskou trombocytopenii, která je téměř vždy lehkého stupně a neohrožuje matku ani plod. Zde léčba není zapotřebí. Jindy je trombocytopenie součástí komplexního závažného onemocnění, které ohrožuje matku i plod na životě, a jedinou kauzální léčbou je včasné ukončení těhotenství (těžké formy preeklampsie, HELLP syndrom, akutní steatóza jater, DIC). Naopak u trombotické trombocytopenické purpury (TTP) ukončení těhotenství nezlepšuje prognózu onemocnění. U léky vyvolané trombocytopenie je indikováno okamžité vysazení léčebného prostředku. U imunitní trombocytopenické purpury (ITP) jsou lékem první volby kortikoidy případně IVIG.
Obecně platí, že léčbu trombocytopenie v průběhu těhotenství zahajujeme, až když počet destiček klesá pod 50 000. To je počet, který vyžadujeme pro bezpečný vaginálně vedený porod. Někteří autoři požadují počet 70 000 pro porod vedený císařským řezem. Trombocytární náplavy použijeme pouze v krajních akutních situacích, kdy hrozí časové prodlení (akutní porod). Nejsou totiž bez rizika. Je zde vyšší riziko aloimunizace v HLA systému, proti HPA (destičkovým antigenům), rizika možného přenosu chorob – virových (CMV, parvovirus B 19) a protozoárních a vzhledem k vyšší skladovací teplotě konzerv (22 °C) i vyšší riziko vzniku septických komplikací způsobených náhodnou bakteriální kontaminací. Dosáhneme-li léčbou dostatečného počtu destiček, plod je dostatečně maturovaný a porodnické cesty jsou dostatečně připravené, je vhodné porod vyvolat indukcí. Naštěstí vzácné jsou trombocytopenie, které vyžadují specifickou léčbu. K nim patří tromboticko trombocytopenická purpura (TTP) a atypický hemolyticko-uremický syndrom (aHUS) a postpartální trombotický mikroangipatický syndrom (PTMS). Zde jediná účinná léčba spočívá v opakovaných plazmaferézách nebo v případě prokázaného aHUS v léčbě pomocí komplementu [1, 3, 7, 8, 14].
IMUNITNÍ TROMBOCYTOPENICKÁ PURPURA
Imunitní trombocytopenická purpura (ITP) komplikuje 1–2 z 1000 těhotenství a podílí se 5 % na příčinách všech tromocytopenií vyskytujících se v průběhu těhotenství. I přes raritní výskyt ve srovnání s gestační tromocytopenií ITP je nejběžnější příčinou izolované trombocytopenie v průběhu prvního a na začátku druhého trimestru gravidity. Patofyziologie ITP je klasicky popisována jako zrychlené odklízení destiček s navázanou IgG anti-trombocytární protilátkou z krevního oběhu. Tyto protilátky rozpoznají specifické epitopy vyjádřené na destičkových glykoproteinech, jako jsou glykoprotein IIb/III a nebo méně často glykoproteiny Ib/IX a Ia/IIa. Tyto destičky s navázanou protilátkou jsou pak vychytávány makrofágy primárně ve slezině [5].
Plod je ohrožen trombocytopenií asi v 10 % případů ITP. Během těhotenství není doporučeno míru trombocytopenie u plodu ověřovat kordocentézou a není z této indikace pro velmi nízké riziko doporučen ani porod císařským řezem. Ihned po porodu odebíráme pupečníkovou krev ke stanovení počtu destiček novorozence a další observace nebo léčba je v kompetenci neonatologa [4, 13].
STANOVENÍ DIAGNÓZY ITP
ITP se v těhotenství prezentuje stejně jako u netěhotných osob. Diagnóza se stanoví detekcí asymptomatické trombocytopenie při rutinním testování a nebo méně často u závažnějších forem onemocnění na základě přítomnosti klinických příznaků, jako jsou tvorba modřin, petechií nebo krvácení. ITP se průběhu těhotenství může zhoršovat nebo zůstane v klidovém stadiu a počet destiček se v průběhu těhotenství nemění. Jedna studie dokládá, že u ITP diagnostikované před těhotenstvím ženy v průběhu těhotenství vyžadují terapii méně často, než ty, u kterých byla ITP diagnostikována nově až v průběhu těhotenství.
Pravděpodobnost, že pacientka trpí ITP víc než náhodnou trombocytopenií, vzrůstá, pokud počet destiček dále klesá, i když není specificky stanoven počet destiček, pod který je možno náhodnou trombocytopenii jednoznačně vyloučit. Navíc u řady pacientek s náhodnou trombocytopenií lze prokázat zvýšenou hladinu k destičkám vázaným IgG, test stanovení protilátek tak nevyloučí tento syndrom. V jedné rozsáhlé studii použili test s monoklonálními protilátkami imobilizující destičkový antigen (MAPA), u méně než 7 % trombocytopenických těhotných žen byly nalezeny autoprotilátky a nebyl nalezen signifikantní rozdíl v prevalenci autoprotilátek mezi trombocytopenickými a non-trombocytopenickými těhotnými ženami.
Tak lze konstatovat, že pro diferenciální diagnózu příčiny trombocytopenie budou důležité anamnestické údaje z prekoncepčního období. Údaje o předchozí atace trombocytopenie, autoimunitním onemocnění nebo závažné trombocytopenii (< 50 000 µl) činí diagnózu ITP více pravděpodobnou. Pokud chybí údaj o počtu destiček před otěhotněním, pak signifikantní trombocytopenie v prvním trimestru s klesajícím počtem krevních destiček v dalším průběhu těhotenství nejvíce konvenuje s diagnózou ITP. Naopak, mírný stupeň trombocytopenie objevující se na konci druhého trimestru nebo ve třetím trimestru spíše konvenuje s gestační benigní trombocytopenií [4, 5].
Mezi jiné důležité údaje řadíme excesivní peripartální krvácení v minulé graviditě nebo trombocytopenii, která se u novorozence objevila záhy po porodu, či výskyt krvácivých komplikací. Vyšetřovací schéma musí zahrnovat vyloučení jiných těhotenských patologií, které jsou provázeny trombocytopenií, jako jsou těžší formy preeklampsie či HELLP syndrom, TTP apod. [6, 9, 12].
Laboratorní vyšetření u těhotné ženy s podezřením na ITP by mělo zahrnovat kompletní krevní obraz, biochemické vyšetření a kompletní koagulační vyšetření. Počet destiček by se měl stanovovat z nátěru na sklíčku a odečítáním pod mikroskopem, tak se vyloučí pseudotrombocytopenie. Laboratorní vyšetření vyloučí i méně frekventní, ale závažné diagnózy, TTP a HUS [9]. Nemělo by se zapomínat ani na možnost HIV nebo HCV infekce. Vyšetření kostní dřeně není v těhotenství doporučeno, u netěhotných žen je však indikováno v případě, že standardní léčba ITP selhává [5].
OBECNÝ MANAGEMENT ITP V PRŮBĚHU TĚHOTENSTVÍ A MOŽNOSTI LÉČBY
Péče o těhotnou s ITP vyžaduje úzkou spolupráci porodníka s hematologem. Stav vyžaduje pečlivé sledování počtu trombocytů jednou za měsíc v průběhu prvního a druhého trimestru, jednou za 14 dnů v průběhu třetího trimestru a pak bezprostředně před porodem. Rozhodnutí o zavedení léčby je podmíněno závažným snížením počtu destiček (< 10 000 nebo < 30 000 ve druhém a třetím trimestru) nebo přítomností krvácivých projevů u pacientky. U asymptomatických pacientek s ITP není nutné bezpodmínečně zvyšovat v průběhu těhotenství počet destiček, doporučeno je zahajovat více agresivní léčbu až později v těhotenství, jako přípravu pacientky pro bezpečný porod.
Kortikosteroidy jsou pro svou účinnost a příznivé finanční náklady léky první volby. Mechanismus jejich účinku spočívá v inhibici fagocytózy napadených trombocytů a potlačení tvorby autoprotilátek. Běžně doporučovaná zahajovací terapeutická dávka prednisonu je 1 mg/kg hmotnosti, která se pak po nástupu léčebné odpovědi snižuje na co nejnižší efektivní dávku. Chronická léčka kortikoidy je spojena pro matku se zvýšeným rizikem rozvoje nežádoucích účinků, jako je rozvoj gestačního diabetu, zvýšení krevního tlaku, ztráta kostní hmoty, přírůstek na hmotnosti a možné abrupce placenty nebo zvýšení rizika předčasného porodu. Léčba kortikoidy v prvním trimestru je některými autory spojována se zvýšeným rizikem vzniku vrozených vývojových vad plodu, především orofaciálních rozštěpových vad. Při vědomí těchto nežádoucích účinků léčby je v praxi u pacientek, u kterých je léčba indikovaná, ale není urgetní, používána v léčbě nízká dávka kortikoidů mezi 20–30 mg/den.
Léčba vysokými dávkami intravenózně podávaného imunoglobulinu (IVIG) 1–2 mg/kg po dobu 2–5 dnů je efektivním způsobem, jak promtně zvýšit počet trombocytů. Efekt léčby je však přechodný a je vhodný u pacientek s těžkou formou trombocytopenie v průběhu třetího trimestru gravidity. Léčba IVIG je finančně velmi nákladná a opakované podání pacientky špatně tolerují, nehodí se tudíž pro dlouhodobou léčbu. Na rozdíl od kortikosteroidů není podávání IVIG spojeno s elevací krevního tlaku.
U pacientek, u nichž samotná léčba kortikosteroidy nebo IVIG selhává a nedosahujeme dostatečné terapeutické odpovědi v podobě zvýšení počtu trombocytů, je doporoučeno podat kombinaci obou léčebných přípravků [4, 5, 10, 11].
Splenektomie je dalším možným léčebným postupem u pacientek, u kterých oba výše popsané léčebné postupy selhaly. Remisi ITP u pacientek po splenektomii můžeme očekávat až v 75 % případů ITP. Splenektomie se provádí v průběhu druhého trimestru, později je to technicky velmi obtížné. Je možné ji provést v těhotenství bezpečně i laparoskopicky.
Jiný publikovaný způsob léčby u pacientek, které nereagují na léčbu kortikoidy nebo IVIG, je podání i.v. anti-D imunoglobulinu v průběhu 2. a 3. trimestru. Bylo dosaženo částečné terapeutické odpovědi a nebyly popsány žádné negativní účinky na matku či plod. Data jsou však velmi omezená, a tak bezpečnost tohoto způsobu léčby není možné jasně posoudit [10].
Ostatní léčebné prostředky používané v léčbě ITP u netěhotných, jmenovitě cytotoxické a imunosupresivní látky, jsou pro svou potenciální teratogenicitu z léčby u těhotných žen vyloučeny (danazol, cyklofosfamid, vinkristin). Azathioprim (Imuran) byl opakovaně podáván u žen po transplantaci ledviny. Nebyly popsány žádné negativní účinky na plod. Nástup účinku lze očekávat v řádu týdnů. Azathioprim může u exponovaných dětí vyvolat hematologický a imunologický útlum, a proto zůstává v kategorii D FDA kategorizace léčebných přípravků. Rituximab byl rovněž opakovaně podáván u těhotných s lymfomem. Ani zde nebyly popsány závažné fetální malformace kromě abnormální tvorby B lymfocytů v prvních šesti měsících života s následnou úplnou úpravou a bez výskytu infekčních komplikací. Obecně tedy zvažovat podání cytotoxických nebo imunosupresivních látek v ojedinělých, zcela individuálních případech závažné formy ITP v průběhu druhého a třetího trimestru, kdy ostatní způsoby léčby selhaly.
Podobně je velmi málo zkušeností s podáváním trombopoetických prostředků v průběhu těhotenství. Eltrombopag a Romiplostin jsou řazeny do katagerie C FDA kategorizace.
Trombocytární náplavy by měly být užity pouze v emergentích případech akutní potřeby ukončení těhotenství [4, 5, 10, 11].
RIZIKO VZNIKU TROMBOCYTOPENIE U PLODU MATEK ITP
Mateřské IgG antitrombocytární protilátky jsou aktivně transportovány do fetální cirkulace a zkříženě reagují s antigeny fetálních destiček. To vede k rozvoji různého stupně fetální trombocytopenie a potenciálně se zvyšuje riziko hemoragie u plodu během porodu. Z rozsáhlé metaanalýzy publikovaných prací vyplývá, že počet trombocytů nižší než 50 000 byl zaznamenán u 10 % novorozenců a počet trombocytů nižší než 20 000 u 4,2 %.
Největší obavy spojené s fetální trombocytopenií představuje riziko vzniku intrakraniálního krvácení, ke kterému teoreticky může dojít při traumatu hlavičky při prostupu porodním kanálem během vaginálního porodu. Navzdory této racionální teorii v praxi se ukázalo toto riziko jako velmi nízké. U výše citované rozsáhlé metaanalýzy nebyl zaznamenán žádný případ intrakraniálního krvácení. Obecně se uvádí, že toto riziko nedosahuje ani 1 %.
Neexistuje korelace mezi počtem mateřských destiček či stupněm závažnosti mateřské ITP a rozvojem trombocytopenie u plodu. Nelze tedy určit korelaci mezi počtem fetálních destiček v době porodu a závažností ITP u matky, a to ani na základě hladiny cirkulujících antitrombocytárních protilátek u matky. Ze zkušeností vyplývá, že ze všech studovaných indicií je nejvalidnější údaj pro stanovení rizika rozvoje fetální trombocytopenie anamnestický údaj o prokázané trombocytopenii v době porodu u dříve narozeného sourozence.
Invazivní procedury k zjištění počtu trombocytů u plodu nejsou doporučovány. Odběr venózní krve z hlavičky plodu je technicky obtížný a dává falešně pozitivní výsledky. Kordocentéza sice poskytne přesné údaje o počtu fetálních trombocytů, ale je zatížená až 2 % komplikací, které si mohou vyžádat akutní ukončení těhotenství [10, 11, 13].
VEDENÍ PORODU
Primární pro bezpečný porod je dosažení dostatečného počtu trombocytů, abychom minimalizovali riziko vážnějšího peripartálního krvácení, a to nejen pro vaginálně vedený porod, ale i pro porod císařským řezem. Běžně používanou metodou porodnické analgezie je epidurální analgezie vyžadující adekvátní hemostázu, aby se minimalizovala rizika neurologických komplikací. Americká hematologická společnost považuje 50 000 destiček za dostatečný počet pro oba způsoby porodu. Britská hematologická společnost vyžaduje pro císařský řez, stejně jako pro epidurální anelgezii 80 000 destiček. Česká gynekologicko-porodnická společnost a Česká hematologická společnost vyžadují pro vaginální porod 50 000, pro císařský řez 70 000 a pro epidurální analgezii 100 000 destiček.
Dříve se věřilo, že císařský řez sníží riziko intrakraniálního krvácení u novorozence. Za poslední dvě až tři desetiletí se neukázalo, že by tomu tak bylo. Císařský řez by měl být proveden jen na základě mateřské indikace nebo z čistě porodnických indikací.
V praxi se osvědčilo koordinovat energickou léčbu s dostatečnou maturací plodu a zráním vaginálního nálezu. Při léčbou dosaženém dostatečném počtu trombocytů, příznivém vaginálním nálezu a dostatečně maturovaném plodu je vhodné vyvolat porod indukcí prostaglandiny.
V poporodním období během prvního týdne života je třeba u novorozence matky s ITP opakovaně sledovat počet trombocytů, protože nástup trombocytopenie způsobený mateřskými protilátkami může být opožděn. Počet destiček se stabilizuje po sedmém dnu života. U novorozenců s počtem destiček < 20 000 nebo s přítomnými krvácivými projevy je indikována léčba IVIG (1 mg/kg hmotnosti). Léčba kortikosteroidy je kontroverzní pro riziko možné predispozice k neonatální sepsi. U dětí s počtem destiček < 50 000 je indikováno sonografické vyšetření mozku případně magnetická rezonance nebo počítačová tomografie. Kojení matkám s ITP nezakazujeme, nebyla prokázána žádná souvislost kojení s trombocytopenií u novorozence [10, 11, 13].
Kazuistika
Pacientkou je dívka ve věku 16 let. V únoru 2016 navštívila svého ambulantního gynekologa se žádostí o hormonální antikoncepci (HAK). Lékař vzhledem k věku žadatelky odebral vzorek krve ke stanovení rezistence k aktivovanému proteinu C (APC–R). Výsledek vyšetření byl pozitivní, lékař HAK nepředepsal a odeslal dívku k hematologickému vyšetření. K hematologickému vyšetření se dívka dostavila v červnu 2016. Bylo prokázáno nosičství leidenské mutace v heterozygotní konfiguraci a trombocytopenie 58×109 imunitní etiologie. Při hematologické kontrole v srpnu 2016 byla již dívka těhotná, ve 20. g.t. Byl prokázán významný pokles trombocytů na hodnotu 14×109. Nasazen byl prednison 20 mg/24 hodin p.o. a pacientka byla odeslána ke konziliárnímu vyšetření do ÚHKT Praha. Krátkodobě byla hospitalizována na ÚHKT Praha v září 2016. Aplikován Solumedrol 40 mg/den i.v. po 2 dny, poté přechod na prednison 50 mg/den p.o. a nasazena profylaktická dávka LMWH (Clexane 0,4 ml s.c. po 24 hod.). Doporučen překlad do spádové nemocnice.
Pacientka byla přijata do perinatologického centra v Mostě klinicky v dobrém stavu bez přítomných krvácivých projevů ve 26. g.t. Vstupní hodnota trombocytů byla 42×109. Pokračovalo se v perorální aplikaci prednisonu v dávce 50 mg/den p.o. Vstupní sonografické a gynekologické vyšetření prokazuje, že plod odpovídá gestačnímu stáří, mozkové struktury jsou bez známek patologie, normhydramnion, hodnoty dopplerovské flowmetrie na pupečníkových cévách a v AMC jsou v normě, palpační vyšetření hodnoceno jako klidový těhotenský nález, kardiotokografie plodu s fyziologickou křivkou.
Během prvních dvou týdnů hospitalizace dochází přes terapii k postupnému poklesu počtu trombocytů až na 26×109 . Po konzultaci s ÚHKT byl vysazen prednison, aplikován jeden den Solumedrol 80 mg/d i.v. a další dva následující dny 40 mg/d i.v. bez terapeutické odezvy. Přistoupeno bylo k aplikaci Kiovigu (IVIG) 40 g po 4 dny. Dochází ke vzestupu počtu trombocytů na 91×109. Po dalších dvou týdnech na počátku října 2016 dochází opět k poklesu počtu trombocytů na hodnotu 22×109. Opět byl nasazen prednison perorálně v úvodní dávce 60 mg s postupným snižováním dávky o 5 mg denně ve snaze udržet počet trombocytů na akceptovatelných hodnotách. Klinicky je pacientka nadále bez jakýchkoliv obtíží, bez jakýchkoliv krvácivých projevů. Přes chronickou medikaci se prohlubuje trombocytopenie, která vrcholí 5. 10. 2016 kritickou hodnotou 1×109. Laboratorní chyba vyloučena opakovaným odběrem. Navíc se u pacientky objevila v laboratoři výrazná anemizace (Hb75 g%) a elevace jaterních enzymů. Vyloučeny byly všechny diagnózy spojené s mikroagiopatickou hemolytickou anémií (MAHA). Ultrazvukové vyšetření vyloučilo odlučování placenty, dopplerovská flowmetrie na umbilikálních arteriích a arteria cerebri media plodu vykazovala normální hodnoty. Klinicky byla pacientka bez známek jakýchkoliv krvácivých projevů. Podány dvě transfuzní jednotky eryroctárních náplavů. Dochází k vzestupu Hb na hodnotu 109 g% a přistoupeno k podání druhé dávky Kiovigu 50 g/den po čtyři dny. Trombocyty stouply na hodnotu 139×109. K další anemizaci již nedochází, krevní obraz při další ferroterapii (maltofer 2×1 p.o.) se drží na hodnotách Hb 11,5 g%. V dalších dnech si pacientka stěžuje na bolest v krku, diagnostikována je streptokoková faringitida, která si vyžádala antibiotickou léčbu Ospenem (fenoxymetylpenicilinum kalcium). Opět dochází k prohlubování trombocytopenie na hodnotu oscilující mezi 5–15×109. Dne 21. 10. 2016 po konzultaci s ÚHKT bylo doporučeno nasadit Imuran (azathioprim) v úvodní dávce 200 mg/den a posléze dávku snížit na 150 mg/den v kombinaci s prednisonem v dávce 20 mg/den. Pravidelné kontroly stavu plodu in utero potvrzují, že plod nadále prosperuje, mozkové struktury plodu jsou bez zjevné patologie. Dne 30. 10. 2016 klesá počet trombocytů na hodnoty kolísající mezi 1–2×109. Po celou dobu hospitalizace pokračuje profylaktické podávání Clexanu v dávce 0,4 ml s.c./24 hod jako prevence tromboembolismu. Je doplněno dopplerovské ultrazvukové vyšetření hlubokého žilního systému dolních končetin s negativním výsledkem. Pacientka je nadále bez krvácivých projevů, opětně konzultováno ÚHKT. Doporučeno je snížit dávku Imuranu na 75 mg/den a uvažovat po patřičné přípravě o ukončení těhotenství.
Dne 2. 11. 2016 byla pacientka po dohodě přeložena do Perinatologického centra Gynekologicko-porodnické kliniky v Ústí nad Labem v gestačním stáří 32+3 k plánovanému ukončení těhotenství per sectionem po hematologické přípravě, ideálně na počátku 34. gestačního týdne. Pacientka při přijetí byla bez klinických obtíží, počet trombocytů ze vstupní laboratoře 24×109, ultrazvukové vyšetření včetně dopplerovské flowmetrie a vstupní kardiotokografické vyšetření vykazovaly fyziologické hodnoty, palpační těhotenský nález byl zcela klidový. V odpoledních hodinách dochází k dramatickému zvratu. Pacientka začala krvácet slabě až středně silně z rodidel. Ihned povolán multidisciplinární tým za účasti dětské hematoložky z dětské kliniky, hematoložky z oddělení klinické hematologie, neonatologa a anesteziologa. Pacientka byla napojena na kontinuální kardiotokograf, provedeno bylo ultrazvukové vyšetření, které neprokázalo známky abrupce placenty. Akutně byly podány dvě transfuzní jednotky trombocytárních náplavů z buffy coatu a aplikováno 50 g Kiovigu i.v. Plod po celou dobu nevykazoval známky intrauterinního stresu. Krvácení z rodidel ustává, počet trombocytů stoupl na 90×109. Ve večerních hodinách se objevuje nová ataka krvácení z rodidel, kardiotokografická křivka nadále bez patologie, kontrolní sonografické vyšetření již prokazuje suspektní známky odlučování placenty. Počet trombocytů již umožňuje přistoupit k akutnímu císařskému řezu.
Operační výkon v celkové anestezii proběhl zcela bez komplikací, krevní ztráta 600 ml. Porozeno bylo děvče 1750 g/42 cm, Apgar skóre 10–10–10. Z pupečníku byla odebrána ihned krev ke stanovení počtu trombocytů u novorozence a placenta odeslána na histologické vyšetření. Novorozenec po celou dobu hospitalizace nevykazoval známky trombocytopenie. Počty trombocytů se pohybovaly nad 240×109 bez jakékoliv tendence k poklesu. Sonografické vyšetření mozkových struktur bez patologie. Pooperační průběh u matky byl rovněž bez komplikací, počet trombocytů čtvrtý pooperační den 180×109. Histologie placenty potvrdila známky abrupce. Podezření, že transport pacientky 60 km sanitním vozem byl možnou vyvolávající příčinou abrupce placenty, se zdá být racionální. Desátý pooperační den byla matka i s dítětem přeložena zpět do perinatologického centra v Mostě. U matky se pokračovalo v chronické medikaci Imuranem v dávce 50 mg/den p.o., prednison 20 mg/den p.o. Novorozenec dále prosperuje a v gestačním stáří 36+1 je propuštěn i s matkou do domácí péče. Matka předána do ambulantní péče ÚHKT a dítě je dispenzarizováno na hematologickém oddělení nemocnice v Lounech. Ve svých třech letech je dítě bez známek ITP.
ZÁVĚR
ITP nepatří mezi časté příčiny trombocytopenie v těhotenství, ale je velmi důležité na ni myslet. Obvykle se projeví již v prvním trimestru těhotenství, ale může se manifestovat kdykoli v průběhu těhotenství. Časná diagnóza a adekvátní léčba zabrání mateřským i neonatálním komplikacím. Ačkoliv je ITP spojen se signifikantním zvýšením incidence neonatální trombocytopenie, závažné komplikace v podobě intrakraniálního krvácení jsou krajně vzácné. Neexistuje korelace mezi závažností mateřské ITP a incidencí míry závažnosti trombocytopenie u plodu. Císařský řez není z důvodu ITP indikován, není prokázáno, že snižuje již tak nízké riziko intarakraniálního krvácení. V léčbě ITP se uplatní kortikoidy a IVIG. Důležité je sledování počtu destiček v prvním týdnu života novorozence.
Diagnóza ITP může být komplikována velkou škálou jiných příčin trombocytopenie v těhotenství. Znalost diferenciálně diagnostických rozdílů příčin trombocytopenie je kruciální pro úspěšný management těhotenství. Nezbytná je úzká spolupráce s hematologem [1, 3, 4, 5, 10, 11, 13].
Akutní těžké formy ITP v těhotenství jsou velmi vzácné. Jsou většinou vyvolány infekčním inzultem nebo zcela raritně, jako velmi pravděpodobně v tomto případě, samotnou graviditou u adolescentky. Pokud se tato těžká forma ITP manifestuje v časných fázích těhotenství, kdy plod je extrémnně nezralý, stojí porodník před volbou těhotenství ukončit, aby neohrožoval matku, ale osud těžce nezralého novorozence je velmi nejistý, nebo se pokusit léčbou ve spolupráci s hematology těhotenství prodloužit do akceptovatelné zralosti plodu a vzít na sebe odpovědnost za možné mateřské komplikace. Pro druhý způsob řešení je nutné zajistit logistické, komplexní odborné, materiální a v neposlední řadě finanční zajištění případu, proto péče o tyto případy patří do gesce perinatologických center. Jak ukazuje námi prezentovaná kazuistika, léčba je nesmírně drahá a není bez rizik. Neočekávaně dramatický závěr případu skončil úspěšně jen díky připravenosti lékařského týmu a možnostem zdravotnického zařízení promtně zajistit potřebné léčebné prostředky.
Doc. MUDr. Tomáš Binder, CSc.
Gynekologicko-porodnická klinika
UJEP a MNUL
Sociální péče 3316 /12A
400 11 Ústí nad Labem
e-mail: tomas.binder@kzcr.eu
Sources
1. ACOG practice bulletin: thrombocytopenia in pregnancy. Number 6, Sept. 1999. Clinical management qudelines for obstetrician-gynecologists. American College of Obstetricians and Gynecologists. Int J Gynecol Obstet, 1999, 67(2), p. 117–128.
2. Boehlen, F., Samii, K., Epieney, M. Management of thrombocytopenia during pregnancy. Rev Med Suisse, 2011, 9(281), p. 340–344.
3. Cines, DB.,Levine, LD. Thrombocytopenia in pregnancy. Blood, 2017, 130(21), p. 2271–2277.
4. Federici, L., Serraj, K., Maloisel, F., Andrés, E. Thrombocytopenia during pregnancy: from etiologic diagnosis to therapeutic management. Presse Med, 2008, 37, p. 1299–1307.
5. Johnson, JR., Samuels, P. Review of autoimmune thromocytopenia: patogenesis, diagnosis and management in pregnacy.Clin Obstet Gynecol, 1999, 42(2), p. 317–326.
6. Magann, EF., Martin, JN. Twelve steps to optimal management of HELLP syndrome. Clin Obstet Gynecol, 1999, 42, p. 532.
7. No authors listed Practice Bulletin No.166: Thrombocytopenia in pregnancy. Obstet Gynecol, 2016, 128(3), p. 43–53.
8. Perepu, U., Rosenstein, L. Maternal thrombocytopenia in pregnancy. Obstet Gynecol, 2013, 3(1):Article 6.
9. Rehberg, JF, Briery, CM., Hudon, WT., et al.Thrombotic thrombopenic purpura masquerading as hemolysis, elevated liver enzymes, low plateles (HELLP) syndrome in late pregnancy. Obstet Gynecol, 2006, 108, p. 817–820.
10. Silver, RM. Management of idiopathic thromocytopenic purpura in pregnancy. Clin Obstet Gynecol, 1998, 41(2), p. 436–448.
11. Stavrou, E., McCrae, KR. Immune thrombocytopenia in pregnancy. Hematol Oncol Clin North Am, 2009, 23(6), p. 1299–1316.
12. Šimetka, O., Klát, J., Gumulec, J., et al. Early identification of women with HELLP syndrome who need plasma exchange after delivery. Transf apheresis Sc, 2015, 2(1), p. 54–59.
13. Uhrynowska, M., Niznikowska-Marks, M., Zupanska, B. Neonatal and maternal thrombocytopenia: incidence and immune background. Eur J Hematol, 2000, 64(1), p. 42–46.
14. Yan, M., Malinowski, AK., Shehata, N. Thrombocytopenic syndroms in pregnancy. Obstet Med, 2016, 9(1), p. 15–20.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicineArticle was published in
Czech Gynaecology

2019 Issue 6
Most read in this issue
- Molární těhotenství z pohledu patologa a klinika
- Prenatálně diagnostikovaný perzistující urachus s pupečníkovou cystou a časným chirurgickým řešením
- Výskyt gestačního diabetes mellitus před zavedením a po zavedení HAPO diagnostických kritérií
- Vliv fyzioterapeutických postupů na zatížení plosky a bolesti zad v těhotenství
